Гиромитрин (Gyromitrin)
Рис.: Гиромитрин (Gyromitrin) Модель
Гиромитрин (Gyromitrin) — азотсодержащее органическое вещество из класса нитрозаминов. Контаминант, является токсином и канцерогеном, присутствующим у представителей родов грибов Gyromitra и Helvella. Он нестабилен и легко гидролизуется до токсичного соединения монометилгидразина. Монометилгидразин действует на центральную нервную систему и препятствует нормальному использованию и функционированию витамина В₆. Отравление приводит к тошноте, спазмам желудка и диарее, в то время как тяжёлое отравление может привести к судорогам, желтухе, коме или даже смерти. Воздействие монометилгидразина обладает канцерогенным эффектом для подопытных животных.
Рис.: Монометилгидразин MMH (CH3NHNH2), токсичный метаболит, модель
При отравлении развивается Гиромитровый синдром. Токсин гиромитрин (N-метил-N-формилэтанал- гидразон), в результате гидролиза образует цитотоксическое соединение N-монометилгидразин, которое способно ингибировать синтез ДНК и РНК, при этом этилен-гиромитрин является наиболее токсичным.
Гидразины образуют в клетках печени нестойкие диазосоединения — источники образования свободных радикалов, а также цитолиза и некрозов в тканях печени.
Наличие органических кислот (фумаровая и др.), кроме поражения печени и почек обуславливает в клинической картине отравлений этими грибами развитие гемолиза и гемоглобинурийного нефроза. При кипячении и длительной сушке (около одного месяца) из-за воздействия кислорода кислоты разрушаются. При вымачивании грибов часть кислот переходит в раствор, но сохраняет токсичность. Таким образом, продолжительное высушивание или длительное отваривание с промывкой позволяют снизить содержание токсичных веществ до относительно безопасного уровня. При этом следует иметь ввиду, что полностью избавиться от токсинов в грибах не удастся.
Считавшаяся ранее ответственной за развитие гемолиза гельвелловая кислота, в настоящее время рассматривается, как лабораторная ошибка.
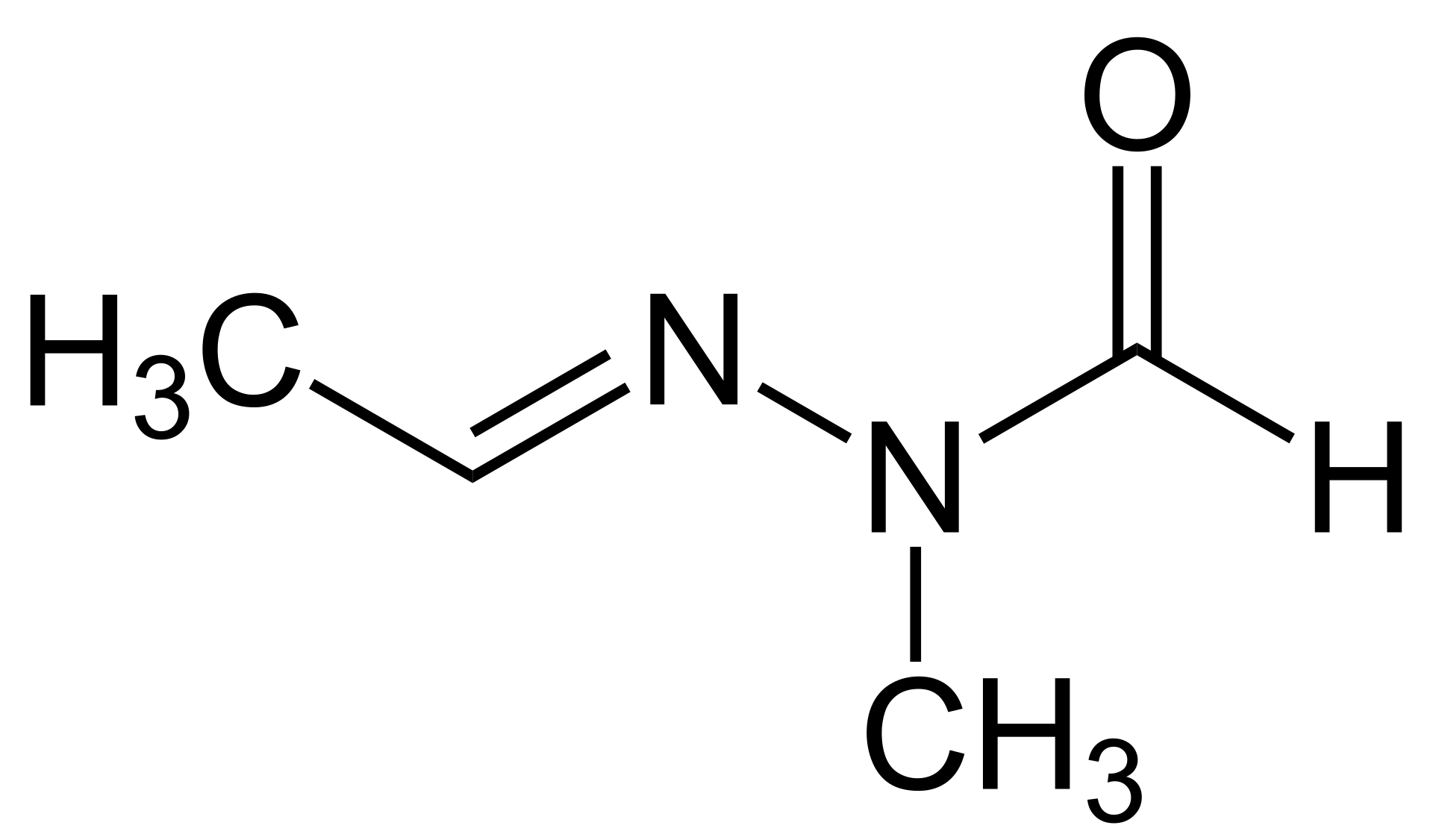
Рис.: Гиромитрин (Gyromitrin) Структурная формула
Для более детального понимания механизма токсикологического воздействия на организм, приведём цитату из научной работы «Современные представления о токсинах высших грибов: простые азотсодержащие соединения» внушительного коллектива учёных из Военно-медицинской академии им. С.М. Кирова (С-Петербург), Государственного научно-исследовательского испытательного института военной медицины (С-Петербург) и Ботанического института им. В.Л. Комарова РАН (С-Петербург), которая была опубликована в научном журнале «Успехи современной биологии», 2020, T. 140, № 4:
Введение
Предполагают, что на Земле может существовать от 1,5 до 3,8 млн. видов грибов, из которых в настоящее время науке известно около 120 тыс., в том числе свыше 27 тыс. макромицетов, то есть видов с крупными плодовыми телами. Из всего изученного биоразнообразия около 500 видов макромицетов ядовиты для человека, а 216 – обладают галлюциногенными свойствами. Состояния, возникающие при отравлении высшими грибами, – мицетизмы (шифры МКБ-10 T 40.9, Т 62.0). Из ядовитых и галлюциногенных грибов на территории России описано порядка 150 видов, что определяет значимость мицетизмов в структуре заболеваемости среди прочих причин пищевых интоксикаций небактериальной этиологии. Несмотря на эволюцию методов анализа и идентификации веществ, токсины макромицетов до настоящего времени мало изучены. Химическая структура идентифицирована не более чем для 5–20% токсинов высших грибов.
Макромицеты представляют собой источники видоспецифических биологически активных простых азотсодержащих соединений. Они могут быть причиной возникновения отдельных нозологий в составе каждой из шести описанных (прим.: в данной работе) групп токсидромов клинической классификации мицетизмов, дополненной в последнее десятилетие несколькими новыми синдромами. В связи с этим необходимо рассмотреть основные токсикологически значимые азотсодержащие соединения высших грибов и современные представления о механизмах их действия. Вследствие тесной связи между распространением ядовитых макромицетов и структуры интоксикаций ими, практический интерес вызывает их биологическое разнообразие, в том числе – на территории нашей страны.
Роль простых азотсодержащих соединений высших грибов в формировании патологических процессов
Несмотря на значимость клинической классификации интоксикаций макромицетами, для понимания вызываемого ими патологического процесса не теряет важности химическая систематизация их токсинов. Простые азотсодержащие соединения макромицетов – разнообразная группа веществ со структурой аминов, нуклеозидов и аминокислот, в том числе непротеиногенных, а также содержащих кислородные (оксоланы) и азотистые (изоксазолы, триптамины, пиридины) гетероциклы. Только часть из них можно рассматривать как алкалоиды в традиционном понимании этого термина.
Токсический эффект некоторых соединений обусловлен структурным сходством с нуклеозидами млекопитающих, что определяет цитотоксические свойства, и с аминокислотами-нейромедиаторами, что сопряжено с нейротоксическими и психодислептическими эффектами. Примером служит сходство нестандартных нуклеозидов клитидина и небуларина с биогенными макроэргами, а непротеиногенных аминокислот высших грибов – с нейротрансмиттерами. Корреляция эффектов токсинов макромицетов со структурой их молекулы описана еще акад. С.В. Аничковым на примере ацетилхолина и мускарина, при этом мускарин в настоящее время – наиболее изученный грибной токсин.
Алкалоиды гиромитринового ряда
К грибным ядам, вызывающим неврологические нарушения, а также гемолиз, поражения печени и почек, могут быть отнесены алкалоиды гиромитринового ряда, похожие по механизму токсичности на гидразин.
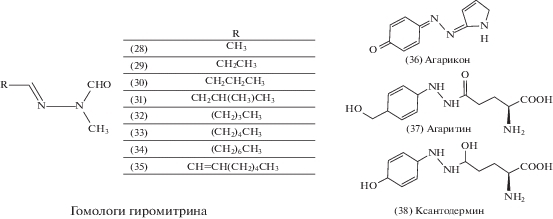
Рис. Химическая структура гиромитрина (28), его гомологов (29–35) и некоторых циклических производных (36–38).
К условно и смертельно ядовитым грибам, содержащим в своем составе гомологи гиромитрина, относят аскомицеты двух семейств порядка Пецицевые (Pezizales):
– семейства Строчковые (Discinaceae): Строчок обыкновенный (Gyromitra esculenta (Pers.) Fr.), С. гигантский (G. gigas (Krombh.) Cooke) и С. осенний, или неприкосновенный (G. infula (Schaeff.) Quél.);
– семейства Лопастниковые (Helvellaceae): Лопастник чашевидный (Helvella acetabulum (L.) Quél.), Л. курчавый (H. crispa (Scop.) Fr.) и Л. белоножковый (H. leucopus Pers.)
Кроме этого, в нашей стране встречаются ядовитые виды, содержащие циклические производные гиромитрина: Шампиньон желтокожий, или карболовый (Agaricus xanthodermus Genev.),
о котором известно, что он имеет в составе агарикон (36) и ксантодермин (38), и Рядовку сросшуюся (Leucocybe connata (Schumach.) Vizzini, P. Alvarado, G. Moreno et Consiglio),
из которой выделили коннатин, псаллиотин и лиофиллин.
Из производных гидразина в съедобном Шампиньоне двуспоровом (Agaricus bisporus J.E. Lange)
выявлен агаритин (37), лишённый острой токсичности. Предполагают, что под действием грибной агаритин-γ-глутамилтрансферазы из агаритина высвобождается 4-метоксиметилфенилгидразин, который далее может окисляться до соответствующей диазониевой соли, способной оказывать канцерогенное действие. При лабораторных испытаниях было прослежено возникновение новообразований у мышей в различных тканях при наличии в их рационе большого количества шампиньонов, содержащих агаритин, однако при аналогичных условиях и дозах самого агаритина канцерогенной активности выявлено не было.
Съедобными двойниками строчков и лопастников может быть род Сморчки (Morchella), которые настолько похожи на первых, что их тоже рассматривают как условно-съедобные, хотя они лишены ядовитых свойств. Примечательным остается факт, что родовой эпитет esculenta – съедобный, получил именно условно-ядовитый G. esculenta.
Гиромитрин – N-этилиден-N-метилформилгидразон (28) в старых изданиях фигурирует как гельвеловая кислота, которая, как изначально считали, была ядовитым началом строчков, что в ходе дальнейших исследований не нашло подтверждений. Концентрация гомологов гиромитрина (29–35) в сушеной массе G. esculenta сильно зависит от климата и возраста макромицета. При этом на долю гиромитрина может приходиться от 0,05 до 0,9%, а на долю метилбутан-гиромитрина (31) – до 2,3% биомассы, в то время как другие производные обнаруживают в следовых количествах.
Острая пероральная токсичность (ЛД50) гиромитрина составляет 344 мг/кг для мышей, 320 мг/кг – для крыс, от 20 до 70 мг/кг – для кроликов. Гибель животных наступает на 2–8 сут. Для человека ЛД50 составляет 25–50 мг/кг для взрослых и 10–30 мг/кг для детей.
В желудке производные гиромитрина подвержены кислотному гидролизу, а в кишке – ферментативной токсификации в метилформилгидразин и монометилгидразин, пик концентраций которых наблюдают в крови через 2 ч после отравления. Так, при внутривенном введении монометил-гидразина собакам ЛД50 составляет 12 мг/кг. Основным путем первой фазы метаболизма гиромитрина и продуктов его гидролиза может быть P450-микросомальное окисление, в результате которого образуются метильные радикалы и нестабильный диазен, играющие основную роль в реализации перекисного окисления липидов, которое на клеточном уровне опосредует цитолитическое и канцерогенное действия. Кроме того, производные гиромитрина вступают в химическое взаимодействие с нуклеиновыми кислотами, образуя ковалентные связи с аминогруппами пуриновых и пиримидиновых оснований, что также оказывает алкилирующее и канцерогенное действия. В сравнении с гиромитринами алифатического ряда, канцерогенное действие у фенил-гиромитринов проявляется в большей степени. В ходе второй фазы метаболизма при участии соответствующих трансфераз происходит конъюгация с эндогенным уридином, фосфатом и ацетатом. В течение суток с мочой элиминирует до 40% гиромитрина, который, обладая диуретическим эффектом, приводит к чрезмерному выведению калия из организма, что, в свою очередь, повышает риск развития электрической нестабильности миокарда.
Попав в кровяное русло, гиромитрин с кровотоком распределяется в органах и тканях, проникает через ГЭБ. Он напрямую связывается с альдегидными группами пиридоксаля, образуя пиридоксаль-гидразоны, которые могут ингибировать пиридоксаль-фосфокиназу (КФ 2.7.1.35), ответственную за превращение провитамина B6 в активный пиридоксаль-5-фосфат. Без кофактора пиридоксаль-5-фосфата декарбоксилаза глутаминовой кислоты (КФ 4.1.1.15) не может преобразовать глутамат в ГАМК в шунте Робертса. По мере истощения пула γ-аминомасляной кислоты стимуляция ГАМК-ионофоров падает, что приводит к снижению судорожного порога.
В результате ингибирования других пиридоксальсодержащих ферментов возникают нарушения обмена, которые на аутопсии косвенно определяют по жировому перерождению всех внутренних органов и тканей. Ингибируя кишечную диаминоксидазу (КФ 1.4.3.6), гиромитрин может приводить к нарушению деятельности энтерогематического барьера и повышению его проницаемости для тканевых ядов и микрофлоры, что может потенцировать риск развития множественной органной дисфункции. В отчетах об отравлениях описаны непостоянная токсичность гиромитрина, влияние повторного потребления содержащих его макромицетов на уровень индивидуальной чувствительности к токсину и наличие идиосинкразии.











Отличная статья! Андрей 3, спасибо за информацию, это очень интересно и очень полезно.